Dr. Alberto Eustáquio Caldeira de Melo – Cardiologia Clínica
Introdução
Prolapso valvular mitral (PVM) ou Síndrome de Barlow é uma anormalidade que afeta em torno de 3,5% da população mundial sendo a mais comum entre todas as valvopatias. Quando o ventrículo esquerdo se contrai, o ajustamento dos dois folhetos que compõem a valva mitral impede o refluxo de sangue para o átrio esquerdo. No PVM ocorre o deslocamento sistólico anormal de um ou ambos os folhetos mitrais para dentro do átrio esquerdo além do plano do anel valvar. Quando importante a regurgitação mitral provocada pela PVM pode levar a insuficiência cardíaca e a anormalidades do ritmo do coração.
Apesar de ser mais freqüente no sexo feminino o PVM apresenta-se com a forma clinica mais grave (insuficiência cardíaca, fibrilação atrial, eventos neurológicos ou isquêmicos) no sexo masculino, inclusive com maior necessidade de correção cirúrgica da anomalia, mas felizmente a grande maioria dos casos é totalmente assintomática e requer apenas controle clínico sem sequer uso de medicamentos.
Etiologia
Degeneração mixomatosa, idiopática, Síndrome de Marfan ,
Ehlers-Danlos , osteogênese imperfeita, pseudoxantoma elástico , distrofia muscular de Duschene, hipertireoidismo ou mesmo cardiomiopatia isquemia.
Quadro clínico
-Sinais e Sintomas:
.A maioria dos pacientes são assintomáticos e assim permanecem por toda a vida.
.Os principais sintomas são: dor torácica atípica, palpitações, tonturas, síncopes, dispneia, fadiga, distúrbios de ansiedade, inclusive relacionadas à Síndrome do pânico.
. As arritmias mais comuns são: ESA(extra-sístole atrial), TPSV(taquicardia paroxística supraventricular), ESV(extra-sístole ventricular), arritmias ventriculares complexas.
. O quadro clínico pode evoluir para insuficiência mitral e consequente insuficiência cardíaca; disfunção ventricular sistólica; ataque isquêmico transitório; AVCI e endocardite infecciosa.
Exame Físico:
Ausculta: deve ser feita com o diafragma do estetoscópio com o paciente na posição supina, em decúbito lateral esquerdo ou sentado. O achado mais importante é o estalido sistólico de refluxo que ocorre imediatamente após a B1. O clique apresenta-se em meso ou telessístole, com timbre mais rude, associado ou não a um sopro sistólico tardio ou holossistólico de regurgitação, melhor audível na área mitral.
. O prolapso valvar e o sopro são mais precoces quando o volume intracavitário é menor (manobra de valsava e posição ortostática e mais tardios quando o volume intracavitário é maior (decúbito e posição de cócoras).
Exames complementares
-Eletrocardiograma:
Não há alterações eletrocardiográficas capazes de predizer o PVM e, em geral, o ECG é normal nos pacientes assintomáticos. Em uma minoria de pacientes assintomáticos e em muitos sintomáticos, o ECG mostra ondas T invertidas ou bifásicas e alterações inespecíficas do segmento ST nas derivações inferiores e ocasionalmente nas derivações laterais.
É comum a presença de vários graus de bloqueios atrioventriculares, bradicardia (devido à disfunção do nó sinusal), arritmias, como as ESA, TPSV, ESV e uma relação muito freqüente entre PVM e Síndrome de Wolff-Parkinson-White. O prolongamento do intervalo QT pode estar associado às arritmias ventriculares mais graves.
-Raio-X tórax:
As alterações radiológicas só se apresentam quando o prolapso se associa a insuficiência mitral. Nesse caso pode-se perceber aumento de AE e/ou VD e VE, dependendo da gravidade da regurgitação.
-Ecocardiograma:
Método ideal para o diagnóstico do PVM. Pacientes com o diagnostico clinico de PVM devem se submeter ao ECODOTT(transtorácico) como também os seus parentes de primeiro grau.
. O deslocamento de um ou ambos os folhetos além de 2 mm acima do ânulo mitral em corte longitudinal paraesternal define o PVM. Quando este deslocamento é superior a 5 mm, o prolapso é definido como “clássico”. Inferior a 5 mm é definido como “não clássico”. Pode ocorrer ou não espessamento das cúspides e insuficiência mitral.
. O Eco-bidimensional é adequado para a identificação e graduação do prolapso. O Doppler é ainda melhor na quantificação do refluxo. Quanto maior a complexidade da lesão, maior o beneficio do ECO 3D transesofágico em relação a todos os outros métodos ecocardiográficos.
*Pacientes que apresentam quadro de arritmias, vertigens, síncopes, desfalecimento ou alterações em ECG, inclusive aumento do intervalo QT devem ser submetidos ao HOLTER e/ou teste de esforço para melhor estratificação de risco.
Tratamento Farmacológico
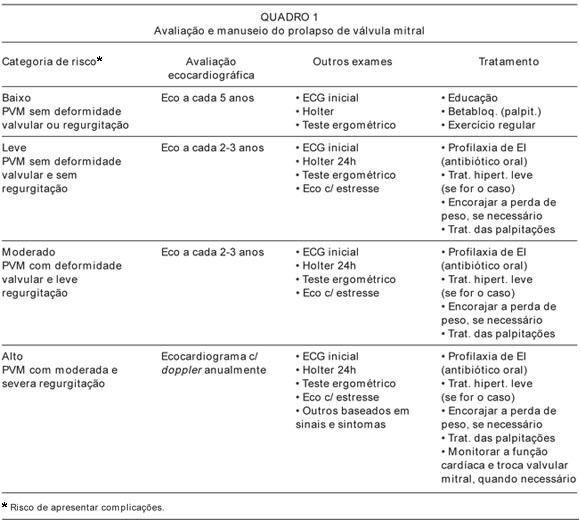
-Pacientes assintomáticos, sem alterações de ECG e sem sinais de regurgitação mitral(RM) devem manter um estilo de vida normal, serem encorajados à pratica de atividades físicas normais e manutenção de boa saúde bucal com consultas de rotina a cada 3 a 5 anos.
– Pacientes com PVM e IM leve a moderada: avaliação clínica e ecocardiográfica pelo menos a cada dois anos
– IM importante e assintomática: no mínimo a cada 12 meses
- A profilaxia da endocardite infecciosa (EI) atualmente não é mais indicada pelas diretrizes da ACC/AHA, mesmo quando associada a insuficiência mitral (IM). No Brasil as poucas estatísticas existentes em centros mais avançados mostram alta incidência de EI em portadores de IM por PVM sendo portanto, mais adequado a indicação da profilaxia para EI para:
– Todos pacientes portadores de valvulopatias anatomicamente significativas, em vez de usar essa estratégia somente para aqueles pacientes considerados de alto risco;
– Procedimentos potencialmente contaminados ou com manipulação de mucosas dos tratos gastrointestinal e geniturinário.
- Frente a presença de arritmias supra-ventriculares ou extrassístoles ventriculares os bloqueadores Beta-adrenergicos são bem indicados. Estas drogas também são úteis nos pacientes que apresentam desconforto torácico associados ou não a doença coronariana.
- O uso de ácido acetilsalicílico (81 a 325 mgs/dia) esta indicado em pacientes com PVM que apresentam eventos neurológicos focais, sem presença de trombos intra-cavitarios ou fibrilação atrial documentada.
- A varfarina com o controle do RNI entre 2,0 e 3,0 está indicada em casos de AIT (acidente isquêmico transitório) recorrentes ou embolia sistêmica documentada. Dose inicial de 5 mgs/dia e em pacientes acima de 60 anos iniciar com metade da dose usual. Outra opção é o rivaroxaban.
PVM associada à IM significativa, com Insuficiência Cardíaca associar:
. Vasodilatador ( IECA: captopril 12,5mg – 1 comprimido VO 8/8 h – aumentar a dose conforme tolerância e determinação clinica) e/ou diurético ( Furosemida 20 a 40mg 24/24 hs ou mais conforme a condição clinica do paciente, na dose máxima diária de 320 mgs/dia). Lembrar a possibilidade de outros IECA (Ação de classe).
- Pacientes com morte súbita recuperada ou taquicardia ventricular sustentada com doença cardíaca estrutural subadjacente: Indicação de CDI
Tratamento Cirúrgico
Frente à necessidade de correção cirúrgica da PVM os critérios de definição de conduta seguem os mesmos adotados na insuficiência mitral, quais sejam:
-Presença de sintomas (NYHA II, III ou IV);
-Disfunção de VE (FE < 60%);
-Remodelamento ventricular esquerdo ( DSF > 40 mm);
-Hipertensão pulmonar grave ou ocorrência de FA durante o acompanhamento clinico.
Estudos observacionais mostram superioridade entre a plastia mitral e a troca valvar mitral. O reparo do folheto posterior tem maior chance de sucesso em relação aos demais folhetos e apresentam alta sobrevida.
Estudos randomizados mostraram a definição estratégica entre cirurgia precoce e o watchful wainting (observação cautelosa) e os dados obtidos mostraram que o watchful waiting é uma estratégia segura para o acompanhamento de pacientes assintomáticos com FEVE e DSF limítrofes(FEVE entre 55 a 60% e DSFVE entre 40 e 55 mm) mantendo como o principal fator desencadeante da indicação cirúrgica o desenvolvimento de sintomas. Portanto, a indicação cirúrgica quando do inicio dos sintomas é altamente aceitável, com baixo risco de complicações, excelente sobrevida pós-operatoria, sendo a pratica mais frequentemente indicada pela maioria das instituições e indicação prioritária das diretrizes.